Vetenskaplig bakgrund
IL1RAP - ett mål av möjligheter
Cantargia utvecklar banbrytande antikroppar som riktar sig mot interleukin‑1‑receptor‑accessory protein (IL1RAP) för att behandla cancer och kroniska inflammatoriska tillstånd. IL1RAP reglerar flera viktiga sjukdomsdrivande signalvägar, och att rikta behandling mot IL1RAP förväntas därför ha signifikant effekt på utvecklingen av flera olika sjukdomar.
IL1RAP i inflammation
IL1RAP är en co-receptor som krävs för signalering nedströms från IL‑1, IL‑33‑ och IL‑36‑receptorerna. När respektive cytokin binder sin receptor rekryteras IL1RAP för att bilda ett aktivt signaleringskomplex som driver inflammatoriska och immunrelaterade signalvägar, främst genom aktivering av NF‑κB och MAPK. IL‑1, IL‑33 och IL‑36 är ofta gemensamt uppreglerade och verkar tillsammans i flera sjukdomar, och blockering av enskilda signalvägar är därför ofta otillräcklig. Genom att blockera IL1RAP med en av Cantargias unika antikroppar är det möjligt att inhibera alla tre IL‑1‑familjens cytokinvägar samtidigt och därigenom uppnå överlägsen effekt vid komplexa sjukdomar.
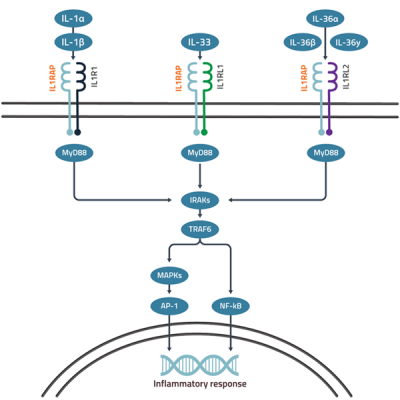
Figur 1. Schematisk översikt av IL-1, IL-33 and IL-36 signalering via IL1RAP.
Den kraftfulla och breda effekten av att blockera IL1RAP har demonstrerats i flera prekliniska modeller av inflammation, och att rikta in sig på IL1RAP har visat sig vara mer effektivt än att blockera enskilda cytokiner (Fig. XX och referenser Lema et al., Fields et al., Grönberg et al., Mulholland et al.). Dessutom har blockad av IL1RAP resulterat ii kraftigt minskad fibros (Fig. XX), vilket utökar möjligheterna för terapier riktade mot IL1RAP från inflammation till att även omfatta fibrotiska sjukdomar.
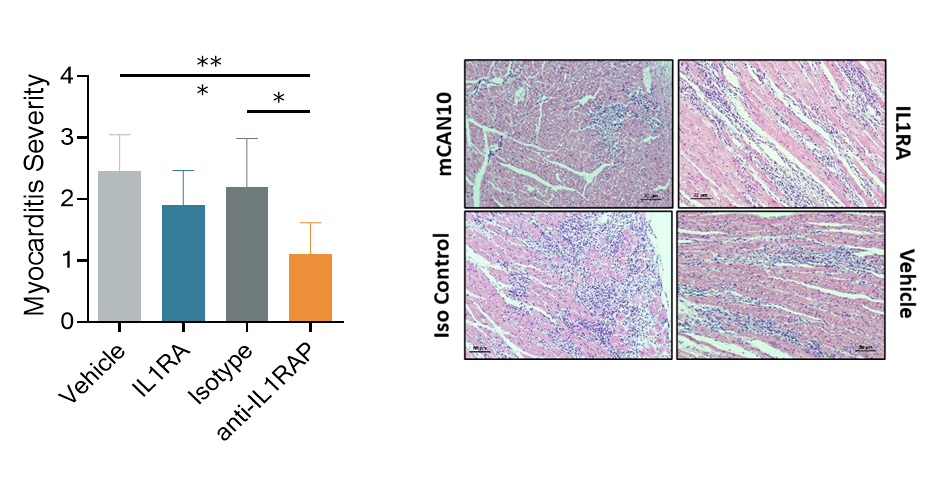
Figur 2. IL1RAP‑blockad minskar hjärtmuskelinflammation i en preklinisk modell av virusinducerad myokardit. IL1RA – blockerar endast IL‑1α och IL‑1β.
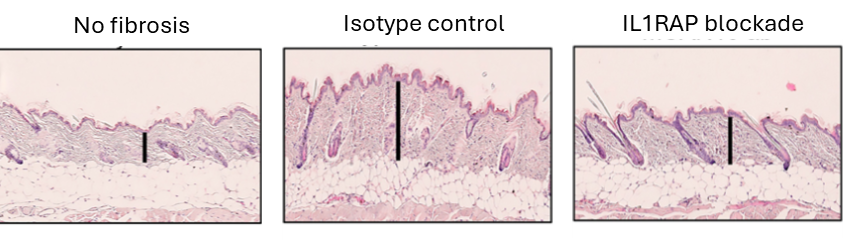
Figur 3. IL1RAP‑blockad minskar fibros i en preklinisk modell av hudfibros.
För att bredda IL1RAP som mål kan det kombineras med en ytterligare funktionalitet i så kallade bispecifika antikroppar för att uppnå potentare effekt anpassad för en viss sjukdom. Detta koncept utreds för närvarande i det så kallade CAN14‑projektet och inom CANxx‑plattformen.
IL1RAP som ett centralt mål inom cancer
Den viktiga rollen för IL1RAP i inflammation är väletablerad, men Cantargias grund bygger på upptäckten att IL1RAP är tydligt överuttryckt i flera olika tumörtyper. Faktum är att höga nivåer av IL1RAP är kopplade till sämre prognos hos patienter med flera cancerformer, inklusive bukspottkörtelcancer (Fig. XX). Detta indikerar att blockering av IL1RAP‑medierad signalering kan vara fördelaktigt vid dessa sjukdomar. Dessutom, tack vare det höga uttrycket av IL1RAP på tumörceller, kan IL1RAP‑riktade antikroppar såsom nadunolimab stimulera kroppens mördar‑celler att hitta och eliminera cancercellerna.
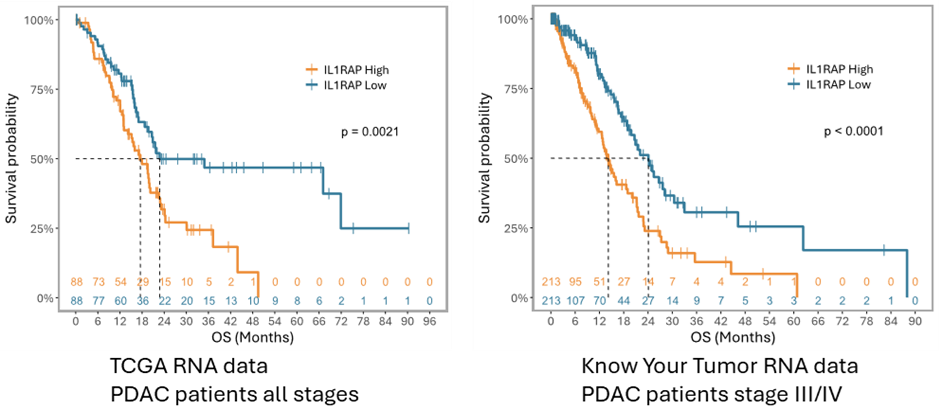
Figur 4. Högt uttryck av IL1RAP är kopplat till sämre överlevnad hos patienter med bukspottskörteltumörer.
IL1RAP finns både på cancerceller och på flera tumörstödjande celltyper i tumörens mikromiljö, inklusive cancerassocierade fibroblaster (CAF). I detta sammanhang är IL1RAP involverat i signalering från framför allt de två IL‑1‑molekylerna, IL‑1α och IL‑1β, som båda bidrar till att skapa en tumörmikromiljö som främjar tumörutveckling och tillväxt. Till exempel kan dessa signaler förstärka tumörens försvarsmekanismer mot de effektorceller som normalt utövar antitumöraktivitet.
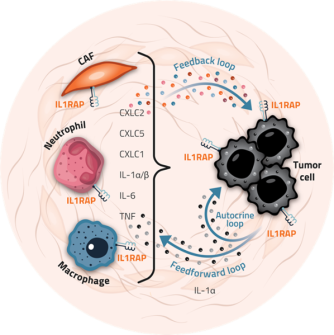
Figur 5. Schematisk översikt av IL1RAP:s roll i tumörmikromiljön i bukspottkörtelcancer. IL‑1 produceras i tumörceller och fungerar som en feedforward‑cytokin som aktiverar myeloida celler och CAFs i tumörmikromiljön. Myeloida celler och CAFs inducerar därefter feedbacksignaler genom att utsöndra mediatorer som stimulerar tumörceller. IL‑1‑familjens cytokiner inducerar även kollagenbildning av CAFs och bidrar till att skapa en fibrotisk, desmoplastisk stroma. Aktiverade CAFs rekryterar dessutom myeloida celler som driver tumörinflammation och skapar en immunhämmande och behandlingsresistent miljö.
Detta innebär att nadunolimab har en dubbel verkningsmekanism – förutom att inducera avdödning av tumörceller blockerar den även tumörfrämjande IL‑1‑signalering. I prekliniska tumörmodeller som inte svarar på immunterapi har det visats att IL‑1 driver systemisk immunsuppression och att blockering av IL1RAP kan återställa ett effektivt antitumörimmunsvar efter immunterapi (ref Hanahan et al.).
Intressant nog kan det höga uttrycket av IL1RAP i tumörer jämfört med normal vävnad också utnyttjas för att leverera terapeutiska cellgifter direkt in i tumörens mikromiljö. Konceptet med så kallade antikropps‑läkemedelskonjugat (ADCs) undersöks för närvarande inom CANxx‑plattformen.

