Våra sjukdomsområden
Cantargias marknadsfokus
Eftersom IL1RAP finns på ett stort antal solida tumörer finns potential att använda Cantargias plattform för behandling av flera former av cancer. Cantargia fokuserar på utvecklingen av sin ledande läkemedelskandidat nadunolimab vid bukspottkörtelcancer (PDAC) samtidigt som möjligheter inom icke-småcellig lungcancer utforskas. Utöver onkologi har interleukin 1 (IL-1) superfamiljen visat sig vara involverad i flera autoimmuna och inflammatoriska sjukdomar. Cantargia har utvecklat antikroppen CAN10, förvärvad av Otsuka Pharmaceutical, och har nyligen tillkännagivit nya bispecifika anti-IL1RAP-projekt inom immunologiområdet.
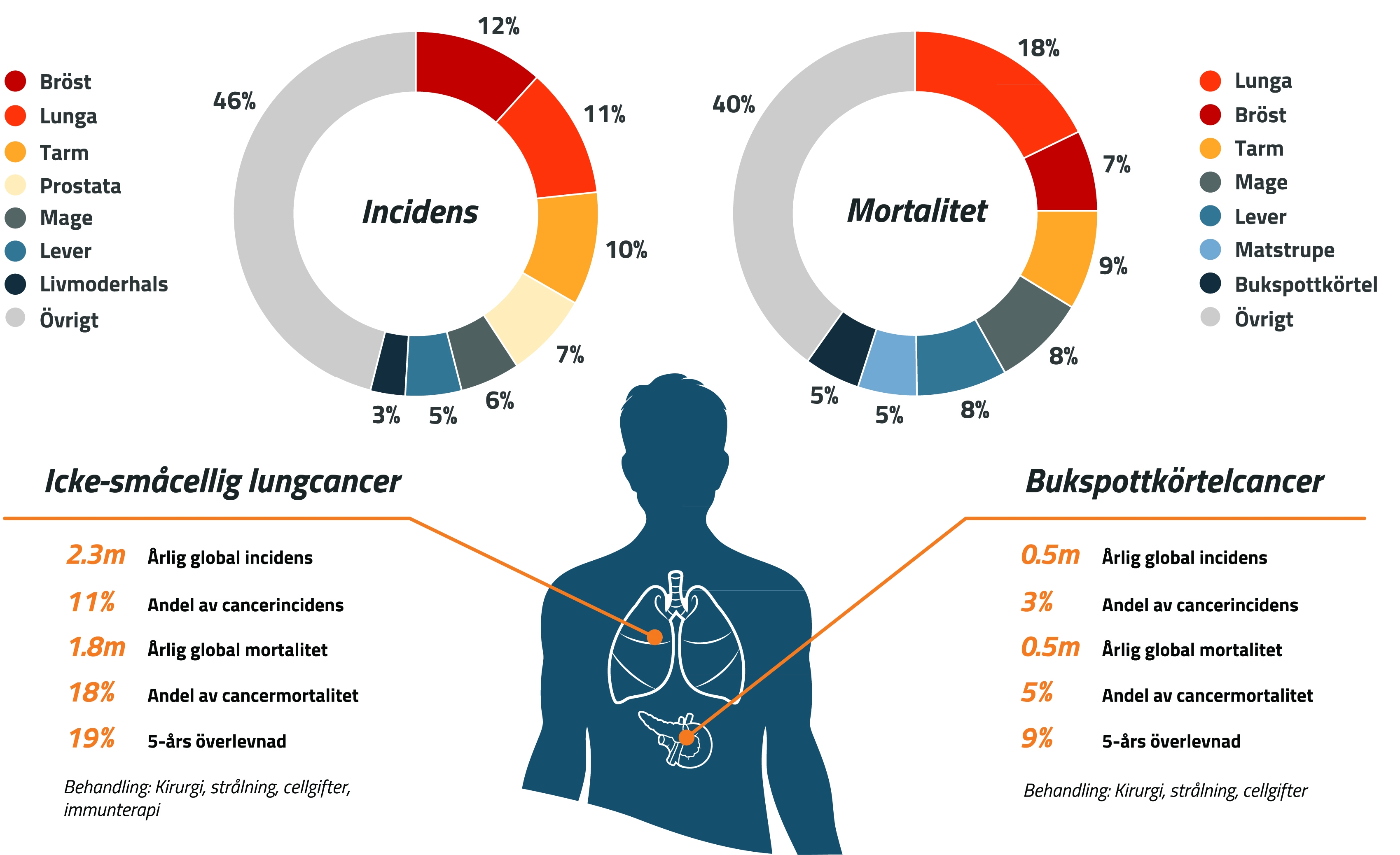
Nadunolimabs marknadspotential
Bukspottkörtelcancer är den 3:e vanligaste orsaken till cancerrelaterade dödsfall i utvecklade länder, inklusive USA och Europa. Antalet patienter som nyligen diagnostiserats med bukspottkörtelcancer under 2024 var cirka 230 000 på de 8 stora globala marknaderna1. Hos 61 procent av dessa patienter hade sjukdomen utvecklats i ett framskridet eller metastaserande stadium2. Baserat på IL1-RAP-uttryck är cirka 85 000 patienter lämpliga för första linjens PDAC-behandling med nadunolimab. Majoriteten av patienterna som behandlas för PDAC får första linjens kemoterapi i olika kombinationer. Under det senaste decenniet har förekomsten av bukspottkörtelcancer ökat, till stor del på grund av den ökande förekomsten av fetma och en åldrande befolkning. Medan den relativa 5-årsöverlevnaden (2015-2021) för alla cancertyper är ca 69 %, är den relativa 5-årsöverlevnaden i PDAC endast 13 %3.
Icke-småcellig lungcancer (NSCLC) är den näst vanligaste cancerformen i världen och den främsta orsaken till cancerdödlighet hos män och kvinnor. Av det totala antalet fall av lungcancer är cirka 85 % av patienterna drabbade av NSCLC-subtypen. Även om NSCLC-patienter diagnostiseras i de senare stadierna av sjukdomen, vilket ofta leder till dålig prognos, har den relativa 5-årsöverlevnaden förbättrats från 16 % år 2000 till 30 % 20174, med en fortsatt positiv trend under 2021.
Utmärkt kommersiell potential för CAN10
Inflammatoriska sjukdomar är tillstånd där kroppens immunförsvar reagerar på en skada eller attack genom att initiera en inflammatorisk process. Inflammation är en del av kroppens naturliga försvarsmekanism och kan aktiveras av infektioner, skador eller autoimmuna reaktioner. Inflammationen läker vanligtvis, men när den blir kronisk kan den leda till allvarliga vävnads- och organskador. Behandling av inflammatoriska sjukdomar syftar ofta till att minska inflammation och lindra symtom. Autoimmuna sjukdomar uppstår när immunförsvaret av misstag attackerar friska celler istället för att skydda dessa. Genom att blockera IL1RAP skapar CAN10 många möjligheter att behandla tillstånd inom inflammations- och immunologiområdet, ett område som har vuxit enormt under de senaste åren. Mer än hälften av alla sjukdomar anses ha en inflammatorisk eller immunologisk komponent, och läkemedel inom immunologi som adresserar en grundläggande fysiologisk orsak till autoimmunitet, såsom CAN10, kan därför tillämpas på många sjukdomar. Immunologi, det näst största terapiområdet i världen efter onkologi, hade en marknadsstorlek på 194 miljarder USD år 20245 och är uppdelat i behandling av autoimmuna och inflammatoriska sjukdomar. Marknaden för autoimmuna sjukdomar uppgick till 214,5 miljarder USD år 2024 och förväntas växa med cirka 14 % årligen fram till 2029. Läkemedel för behandling av inflammatoriska sjukdomar nådde en marknadsstorlek på 38,7 miljarder USD år 2024, vilket förväntas växa med cirka 4 % årligen fram till 2029.
Marknaden för bispecifika antikroppsterapier och ADC:er
Marknaden för bispecifika antikroppar växer snabbt, driven av en ökad användning inom både onkologi och inflammatoriska sjukdomar. Denna marknadsdynamik speglar ett betydande skifte mot bispecifika antikroppar som centrala komponenter i framtida behandlingsstrategier. Deras dubbla målsökande förmåga kan potentiellt ge förbättrad effektivitet, säkerhet och användarvänlighet jämfört med befintliga terapier. Marknaden för bispecifika antikroppar förväntas expandera med cirka 30 miljarder USD fram till 2030, vilket gör den till en betydande drivkraft bakom den totala tillväxten på antikroppsmarknaden. Samtidigt fortsätter ADC-marknaden att uppvisa ett starkt kommersiellt och vetenskapligt momentum. Det växande intresset inom läkemedelsindustrin för IL1RAP speglar den bredare expansionen inom området, drivet av fortsatt innovation och ökande kliniska framgångar. Bidragande faktorer till den växande ADC-marknaden är den höga anpassningsförmågan hos ADC-läkemedel inom bröstcancer, det dominerande försäljningssegmentet för ADC, den nuvarande och framtida försäljningen av ADC-storsäljare som Enhertu (Daiichi Sankyo/ AstraZeneca), Kadcyla (Roche) och Trodelvy (Gilead), samt det kraftigt ökande antalet ADC-kandidater i utveckling, stärkt av det ökande intresset för strategiska investeringar från stora läkemedelsföretag. Medan den globala antikroppsmarknaden förväntas växa med 200 miljarder USD fram till 2030, drivet av både nya godkännanden (36 FDA-godkännanden under de senaste 3 åren) och utökade indikationer, kommer cirka 10% (eller 20 miljarder USD mellan 2025 och 2030) av denna tillväxt att komma från expansionen av ADC-segmentet, vilket återspeglar dess ökande roll inom onkologi och andra terapiområden med stort marknadsvärde
1 USA, EU-4, Storbritannien, Kina, Japan, globala data, 2025
2 Stadium III icke-resektabel/stadium IV (exklusive patienter som progredierar från tidigare stadier)
3 SEER-data om relativ 5-årsöverlevnad, 2015–2021, alla stadier
4 SEER-data om relativ 5-årsöverlevnad, 1975–2021, alla stadier
5 Immunology at an inflection point: Opportunities & challenges for innovators seeking growth in an unforgiving market, IQVIA 2025.

