CANFOUR
CANFOUR
CANFOUR, den första kliniska studien för nadunolimab (CAN04), är en kombinerad fas I/IIa-studie. I initiala fasen av CANFOUR var syftet att studera säkerhet av CAN04 för att fastställa lämplig dos för den andra delen av studien där behandlingseffekt och säkerhet av CAN04 utvärderas i kombination med cellgifter.
Läs mer om CANFOUR på ClinicalTrials.gov (NCT03267316).
Fas I: Doseskalering och säkerhetsutvärdering - Avslutad
- Inkluderade 22 patienter med bukspottkörtelcancer (PDAC), icke-småcellig lungcancer (NSCLC) eller tjocktarmscancer.
- Resultaten visade att CAN04 har en hög säkerhet och positiva effekter på biomarkörer kopplade till cancer observerades:
- God säkerhetsprofil upp till 10 mg/kg
- Minskning i biomarkörerna IL-6 och CRP
- Stabil sjukdom i 43% av patienterna
- Resultaten från fas I-delen publicerades i British Journal of Cancer i december 2021 och finns att hitta här.
Fas IIa: Utvärdering av terapeutisk effekt - Pågående; rekrytering avslutad
- Utvärderar CAN04 i kombination med cellgifter i patienter med PDAC (första behandlingslinjen med gemcitabin/nab-paclitaxel), NSCLC (första el. andra behandlingslinjen med cisplatin/gemcitabin) eller icke-skivepitel NSCLC (första el. andra behandlingslinjen med carboplatin/pemetrexed).
- Totalt 76 PDAC-patienter har rekryterats (36 i en primärkohort, 40 i en expansionskohort).
- Totalt 43 NSCLC-patienter har rekryterats (33 i kombination med cisplatin/gemcitabin, 10 i kombination med carboplatin/pemetrexed).
Positiva interimsdata från fas IIa för kombinationsterapi i patienter med PDAC - Presenterades på AACR 2023
- Totalöverlevnaden i de 73 PDAC-patienter behandlade med CAN04 och gemcitabin/nab-paclitaxel var 12,9 månader i median, vilket är väsentligt högre jämfört med historiska data för enbart cellgifter [1].
- Ännu starkare effekter uppnåddes i patienter med höga tumörnivåer av IL1RAP, målproteinet för CAN04, bland annat en signifikant förlängd totalöverlevnad jämfört med patienter med låga IL1RAP-nivåer (14,2 vs 10,6 månader; p=0,017).
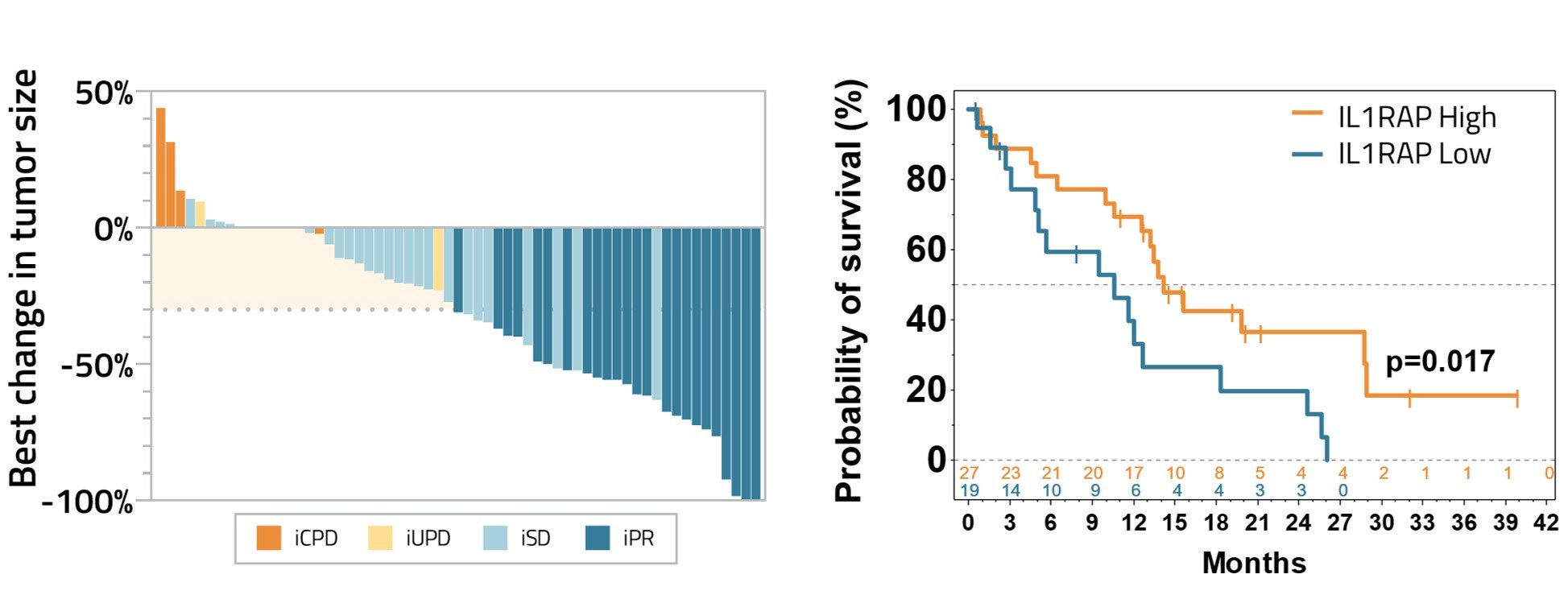
Tumörresponser enligt iRECIST (vänster); total överlevnad för de 46 PDAC-patienter för vilka tumörbiopsier tagits och patienterna grupperats baserat på tumörnivå av IL1RAP (höga, n=27; låga, n=19) (höger).
Effektparametrar för den totala gruppen PDAC-patienter, de två subgrupperna baserat på tumörnivå av IL1RAP, samt historiska kontrolldata.
- Säkerhetsprofilen för kombinationen med gemcitabin/nab-paclitaxel påminner om den som förväntas för enbart cellgifter:
- Förekomsten av neutropeni och febril neutropeni var högre primärt under första behandlingscykeln jämfört med vad som förväntas för enbart cellgifter.
- Vid profylaktisk G-CSF-behandling uppvisade enbart 14% av patienterna neutropeni av grad 3-4, jämfört med 78% utan profylaktisk G-CSF-behandling.
- Förekomsten av neuropati av grad 3-4 var enbart 1%, jämfört med 17% som tidigare rapporterats för cellgifter [1].
Positiva interimsdata från fas IIa för kombinationsterapi i patienter med NSCLC - Presenterades på ASCO 2023
- I de 30 NSCLC-patienter behandlade med CAN04 och cisplatin/gemcitabin var responsfrekvensen 53%, med totalöverlevnad och progressionsfri överlevnad på 13,7 respektive 7,0 månader i median. Dessa data är starkare än historiska data för enbart cellgifter [2-4].
- Den starkaste effekten observerades i de 16 patienter med icke-skivepitel NSCLC med totalöverlevnad på 15,9 månader i median.
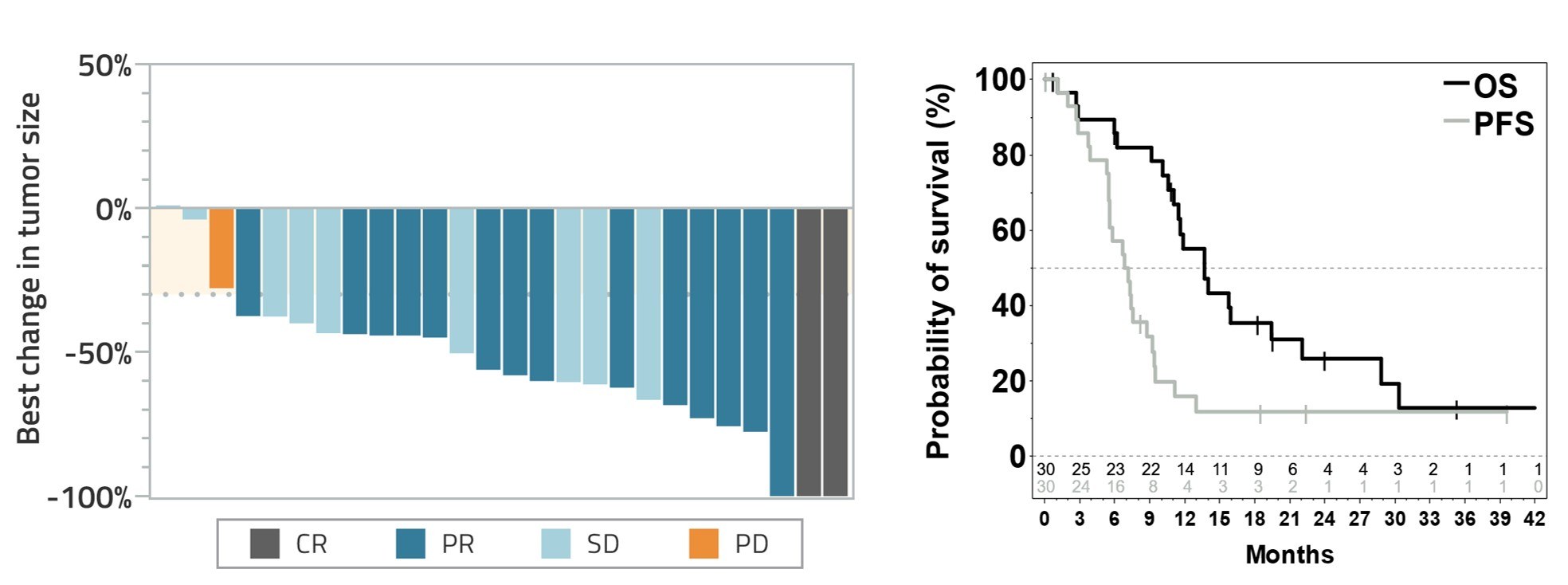
Tumörresponser enligt RECIST (vänster), samt total överlevnad (OS) och progressionsfri överlevnad (PFS) för samtliga 30 NSCLC-patienter (höger).
Effektparametrar för den totala gruppen NSCLC-patienter, icke-skivepitel-subgruppen, samt historiska kontrolldata.
- Bland de 16 patienterna med icke-skivepitel NSCLC, hade två patienter komplett respons; båda hade tidigare slutat svara på Keytruda® och saknade PD-L1 på sina tumörceller.
- En av de kompletta responserna uppnåddes efter nästan 9 månader monoterapibehandling med CAN04 som gavs efter att cellgiftsbehandling avslutats, medan den andra hade ett snabbt behandlingssvar på kombinationen som varat över 3 år.
- Säkerheten av kombinationen var god och hanterbar:
- Frekvensen av neutropeni och febril neutropeni var högre primärt under första cykeln jämfört med historiska data för enbart cellgifter [2].
- Med profylaktisk G-CSF-behandling utvecklade enbart 33% av patienterna neutropeni av grad 3-4, vilket är i nivå för enbart cellgifter, jämfört med 71% utan profylaktisk G-CSF-behandling.
Referenser
[1] von Hoff et al, N Engl J Med 2013; 369:1691-1703
[2] Schiller et al, N Engl J Med 2002; 346:92–98
[3] Scagliotti et al, J Clin Oncol 2008; 26:3543–3551
[4] Gandhi et al, N Engl J Med 2018; 378:2078-2092